Không hiểu sao Vaccine Covid-19 “made in Việt Nam” ít ghi nhận tác dụng phụ nguy hiểm đến thế?
Nói về vắc xin Covid-19 của Việt Nam, GS.TS Trương Việt Dũng nhận định: “Chúng ta đang tiến nhanh những bước cuối cùng để đến vạch đích thành công”.
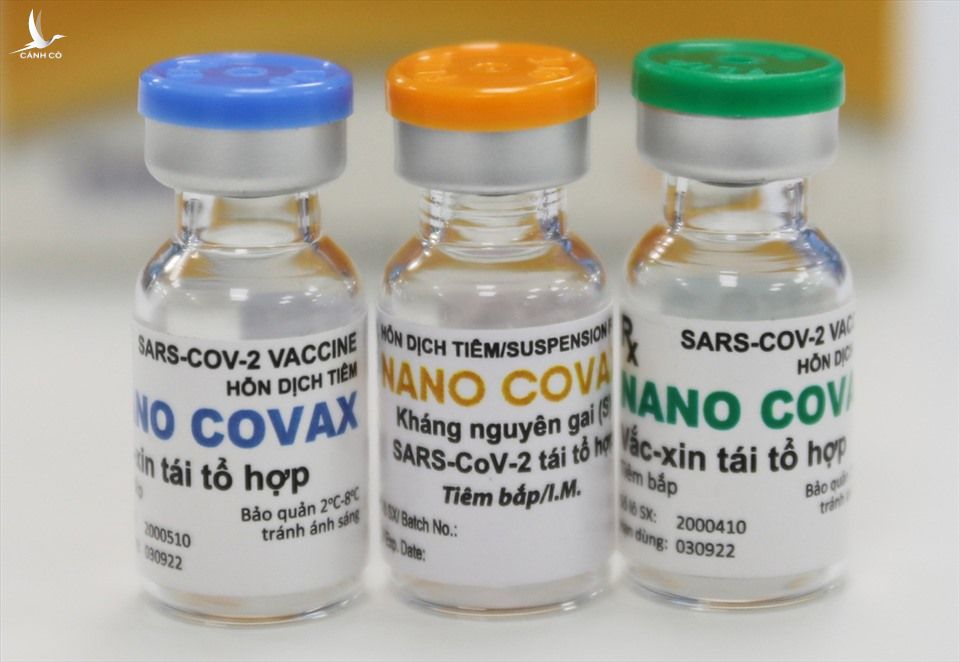
Trong cuộc trao đổi gần đây với chúng tôi, GS.TS Trương Việt Dũng, Chủ tịch Hội đồng Đạo đức quốc gia trong nghiên cứu y sinh học, chia sẻ về vắc xin Nano Covax của Việt Nam: “Tôi không hiểu sao lại ghi nhận ít tác dụng phụ nguy hiểm thế, thậm chí an toàn hơn các loại đang tiêm”.
Sau khi đọc hồ sơ báo cáo kết quả thử nghiệm giai đoạn 2 của Nano Covax, niềm tin của GS. Dũng về sự thành công của vắc xin phòng Covid-19 do Việt Nam sản xuất đang lớn hơn bao giờ hết. “Chúng ta đang tiến nhanh những bước cuối cùng để đến vạch đích thành công”, GS Dũng nói.
PV: Vắc xin Nano Covax đã gửi hồ sơ báo cáo kết quả thử nghiệm giai đoạn 2, xin thực hiện giai đoạn 3 còn vắc xin Covivac cũng đang hoàn thiện hồ sơ kết quả của giai đoạn 1 để báo cáo hội đồng xin chuyển sang thử nghiệm giai đoạn 2. Đến thời điểm này chúng ta đã có thêm những đánh giá như thế nào về các vắc xin do Việt Nam nghiên cứu phát triển thưa Giáo sư?
GS. TS. Trương Việt Dũng: Cá nhân tôi đánh giá tất cả các chỉ số từ bản báo cáo kết quả giữa kỳ giai đoạn 2 của Nano Covax đang cho thấy không có vấn đề gì phải quan ngại về vắc xin này. Tính an toàn của vắc xin rất tốt với tỷ lệ sốt sau khi tiêm dưới 2%. Thậm chí nó còn an toàn hơn các loại vắc xin mà mình đang tiêm hiện nay.
Bên cạnh đó, vắc xin Covivac cũng vừa tiêm xong cho tất cả các tình nguyện viên và đang gửi mẫu sang phòng thí nghiệm ở nước ngoài để làm các đánh giá miễn dịch. Quá trình tiêm thử nghiệm giai đoạn 1 của vắc xin này, phải nói chính chúng tôi cũng không hiểu tại sao mà nó ghi nhận rất ít tác dụng phụ nguy hiểm đến thế. Nguy hiểm trầm trọng không có đã đành, ghi nhận tác dụng phụ mức độ nặng cũng rất ít, gần như không có. Thường chỉ nhận thấy các dấu hiệu sưng, nóng, đỏ, đau, hơi sốt ở 1 – 2 ngày sau tiêm. Và những biểu hiện thường thấy như vậy thì ta nên vui mừng.
Tuy nhiên, phải nhìn nhận một cách tỉnh táo rằng số lượng người thử nghiệm của mình đang ít. Các đợt thử nghiệm vừa rồi của cả hai loại vắc xin Việt Nam đang phát triển mới tiêm được vài trăm người. Trong vắc xin của người ta thì đã có số liệu tiêm trên diện rất lớn, hàng vài chục triệu người rồi.
Hơn nữa, thực tế là chưa có một cộng đồng nào tiêm được đến mức 70 – 80% dân số với cùng một loại vắc xin phòng Covid-19. Và cũng chưa có cộng đồng nào thoát được dịch để có thể chứng minh tính miễn dịch cộng đồng của chính loại vắc xin ấy. Nói chung tất cả các loại vắc xin trên thế giới bây giờ đều trong giai đoạn thử nghiệm. Kể cả những quốc gia đang tiến hành nới lỏng bớt các biện pháp giãn cách, đó cũng chỉ là bước thử nghiệm vắc xin của họ trên diện rộng.
Cho nên phát triển vắc xin lúc này người ta chỉ quan tâm nhất đến vấn đề có an toàn hay không. An toàn ở đây không có nghĩa là tỷ lệ tử vong hay những thông tin về người chết sau tiêm chủng. Những phản ứng phụ mà cuối cùng dẫn đến tử vong thì các vắc xin thông thường – được nghiên cứu và kiểm nghiệm trong suốt 10 năm cũng đều có phần triệu xác suất đấy.
Ví dụ ngay như vắc xin của AstraZeneca, họ thông báo tỷ lệ tử vong chiếm cỡ 4 – 5 phần triệu. Nghĩa là khoảng 1 triệu người tiêm thì có từ 4 – 5 người phản ứng phụ dẫn đến mức tử vong. Phải tiêm được hàng chục triệu người ta mới có được số liệu đó. Nhìn lại các vắc xin mình đang phát triển biết thử đến liều thứ bao nhiêu để cho ra được tỷ lệ người chết trên triệu người nào. Cho nên nghiên cứu, thử nghiệm đến giai đoạn nào thì chúng ta đánh giá hoặc vui mừng hoặc hy vọng ở giai đoạn ấy.
PV: Thời gian để Hội đồng thẩm định hồ sơ đánh giá và xin chuyển giai đoạn thử nghiệm thường kéo dài bao lâu thưa Giáo sư?
GS. TS. Trương Việt Dũng: Thời điểm này chỉ cần các đơn vị nghiên cứu nộp hồ sơ lên, sau độ 1 tuần Hội đồng sẽ trả lời xong.
Trước đây thì cứ phải hàng tháng để Hội đồng xem xét. Xét xong rồi 1 tháng sau đơn vị thực hiện mới lại sửa và trình lại. Thế là mất 2 tháng rồi còn gì. Trong tình trạng cấp bách khi có đại dịch như thế này, quan điểm của Hội đồng là không vì các thủ tục hành chính mà làm chậm tiến độ.
Cho nên chúng tôi yêu cầu các nhà khoa học phải thật tập trung vào khâu viết đề cương cho đầy đủ, chi tiết. Khi đưa ra Hội động là được Hội đồng làm việc ngay, có kết quả ngay. Như vậy thay vì 2 tháng trời ta rút ngắn xuống còn chậm nhất cỡ 7 ngày.
Thế giới cũng đang phát triển vắc xin Covid-19 theo chiến lược này. Người ta gọi là những “thiết kế nghiên cứu thích ứng”. Nghĩa là anh làm từng giai đoạn 1, rồi anh cuốn chiếu. Ví dụ như cần làm thử nghiệm diện rộng trên 30.000 người chẳng hạn. Anh có thể chia nhiều giai đoạn. Giai đoạn đầu làm trên 1.000 người cho kết quả tốt, anh có thể thay đổi đề cương ấy đi rồi báo cáo kết quả. Cứ như thế cuốn chiếu theo từng giai đoạn nhỏ. Vậy là giúp rút ngắn được thời gian rất đáng kể.
Việt Nam đang đi đúng theo hướng đó, rút ngắn thời gian và thủ tục hành chính chứ kiên quyết không rút bất kỳ giai đoạn nào cả. Mình phải rất chặt chẽ chỗ đó. Nhanh cũng phải đúng nguyên tắc khoa học. Chứ Hội đồng không bao giờ châm chước chuyện đề cương chưa xong điểm này điểm kia mà đã cho làm. Không có đâu! Rút ngắn giai đoạn có mà chết à. Khi trình bày vắc xin ra người ta cười cho. Ai tin mà dùng. Mình làm không khác 1 ly 1 tý nào với tiêu chuẩn của quốc tế cả.
PV: Đơn vị thử nghiệm đang kỳ vọng sớm có thể thực hiện giai đoạn 3 để hướng đến mục tiêu, cuối năm 2021, vắc xin sẽ được cấp phép sản xuất. Tiến độ này khả thi không thưa Giáo sư?
GS. TS. Trương Việt Dũng: Nói chung là có thể được.
Các nhà phát triển đã rất nỗ lực, các đơn vị thử nghiệm thì đầu tư đầy đủ mọi điều kiện thuận lợi nhất để triển khai. Con đường đi của vắc xin này đang rất khả quan. Bởi vì, yếu tố quan trọng nhất là sự an toàn thì đã bước đầu chứng minh được. Còn tính phát sinh miễn dịch thì tất cả các vắc xin phòng Covid-19 trên thế giới hiện giờ cũng đều chỉ ở tầm vừa phải thôi. Không phải tất cả vắc xin đều hiệu quả 100%.
Sau khi xét tính sinh kháng thể, người ta mới quan tâm đến tính bảo vệ của vắc xin. Qua giai đoạn 2 cho thấy, Nano Covax đạt hiệu quả sinh kháng thể tốt nhất khoảng trên 90%. Với chỉ số vàng là trung hòa virus sống hay còn gọi là tính bảo vệ thì họ đang phối hợp với Viện Vệ sinh dịch tễ Trung ương để đánh giá.
Vì sao gọi chỉ số trung hòa virus sống là tỷ lệ vàng? Vì thực tế đã chứng mình, nhiều loại vắc xin sinh kháng thể rồi nhưng không có khả năng bảo vệ. Người nhiễm HIV cũng có kháng thể rất nhiều nhưng không có tính bảo vệ đấy thôi. Cho nên chúng ta không làm được vắc xin HIV là vì thế. Có kháng thể mà không bảo vệ được cơ thể. Thời điểm này muốn biết 1 vắc xin có mức độ bảo vệ như thế nào thì cần phải làm những phản ứng trung hòa trên virus sống. Làm những phản ứng loại này rất đắt tiền. Đòi hỏi phải đến những phòng thí nghiệm đặc biệt, có độ an toàn sinh học cấp 3 mới làm được.
Nhắc đến chỉ số vàng này tôi phải nói rất mừng, ngoài Nano Covax ra còn 1 loại vắc xin cũng do Việt Nam phát triển là Covivac đang có được bộ hồ sơ về các phản ứng này rất tốt. Ivac nhà phát triển của Covivac đã làm các chỉ số này rất cẩn thận. Họ không phải là những người vội vã đâu. Ngay từ đầu mọi chỉ số đánh giá họ đều gửi sang các phòng thí nghiệm uy tín của Mỹ để làm. Như vậy đồng nghĩa với việc, các chỉ số đó đã có được bảo chứng của quốc tế.
Cho nên cơ hội để đi đến chuyện được cấp phép là rất rộng mở đối với các vắc xin do Việt Nam phát triển.
PV: Trong trường hợp được cấp phép thì năng lực sản xuất vắc xin của Việt Nam liệu có đáp ứng được với nhu cầu hiện nay không thưa ông?
GS. TS. Trương Việt Dũng: Việc vắc xin Nano Covax được duyệt cấp phép hay không còn phụ thuộc vào kết quả thử nghiệm giai đoạn 3 tới đây. Tuy nhiên nhà sản xuất và nhóm nghiên cứu đã chuẩn bị sẵn sàng nguyên liệu, các quy trình để có thể đưa vào sản xuất khi được Bộ Y tế phê duyệt, cấp phép. Năng lực sản xuất vắc xin này Việt Nam hiện đang báo cáo là 6 triệu liều/tháng.
Còn với vắc xin Covivax, hiện Ivac đang sở hữu dây chuyền sản xuất vắc xin theo tiêu chuẩn quốc tế với công suất 6 triệu liều/năm. Đây là nhà máy được WHO tài trợ xây dựng với tổng kinh phí 2,7 triệu USD cho nên dây chuyền của họ tốt lắm. Chúng tôi đã đến khảo sát nhiều lần và đánh giá vắc xin của họ làm chất lượng nghiêm chỉnh, rất bài bản, đáp ứng hoàn toàn với tiêu chuẩn sản xuất vắc xin của WHO. Thời điểm này Ivac lại đang cho nhập và lắp đặt thêm trang thiết bị để nâng công suất lên thành 30 triệu liều/năm. Như vậy có thể thấy, với sự hỗ trợ từ quốc tế Việt Nam đã có những sự chuẩn bị sẵn sàng cho các tình huống phát sinh đại dịch.
PV: Xin cảm ơn GS. TS Trương Việt Dũng!
Thanh An




